صوديوم
| ||||
|---|---|---|---|---|
 | ||||
| اتسمى باسم | صداع | |||
| المكتشف | همفرى ديفى [1] | |||
| تاريخ الاكتشاف | 1807[1] | |||
| الرمز | Na[2] | |||
| الصيغه | Na | |||
| مواصفات الادخال النصى المبسط للجزيئات | [Na] | |||
| العدد الذرى | ||||
| توزيع الكترونى | 1s² 2s² 2p⁶ 3s¹، و[Ne] 3s¹ | |||
| الكتله | ||||
| السالبيه الكهربيه | ||||
| المعيار الحرارى المولى | ||||
| رمز يونيكود | 鈉[3] | |||
| تعديل |
||||
| |||||||||||||||||||||||||||||
| المظهر | |||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
رمادي فلزي الخطوط الطيفية للصوديوم | |||||||||||||||||||||||||||||
| الخواص العامة | |||||||||||||||||||||||||||||
| الاسم، العدد، الرمز | صوديوم، 11، Na | ||||||||||||||||||||||||||||
| تصنيف العنصر | فلز قلوي | ||||||||||||||||||||||||||||
| المجموعة، الدورة، المستوى الفرعي | 1، 3، s | ||||||||||||||||||||||||||||
| الكتلة الذرية | 22.98976928 غ·مول−1 | ||||||||||||||||||||||||||||
| توزيع إلكتروني | Ne] 3s1] | ||||||||||||||||||||||||||||
| توزيع الإلكترونات لكل غلاف تكافؤ | 2,8,1 (صورة) | ||||||||||||||||||||||||||||
| الخواص الفيزيائية | |||||||||||||||||||||||||||||
| الطور | صلب | ||||||||||||||||||||||||||||
| الكثافة (عند درجة حرارة الغرفة) | 0.968 غ·سم−3 | ||||||||||||||||||||||||||||
| كثافة السائل عند نقطة الانصهار | 0.927 غ·سم−3 | ||||||||||||||||||||||||||||
| نقطة الانصهار | 370.87 ك، 97.72 °س | ||||||||||||||||||||||||||||
| نقطة الغليان | 1156 ك، 883 °س | ||||||||||||||||||||||||||||
| النقطة الحرجة | (قيمة حسابية) 2573 ك، 35 ميغاباسكال | ||||||||||||||||||||||||||||
| حرارة الانصهار | 2.60 كيلوجول·مول−1 | ||||||||||||||||||||||||||||
| حرارة التبخر | 97.42 كيلوجول·مول−1 | ||||||||||||||||||||||||||||
| السعة الحرارية (عند 25 °س) | 28.230 جول·مول−1·كلفن−1 | ||||||||||||||||||||||||||||
| ضغط البخار | |||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||
| الخواص الذرية | |||||||||||||||||||||||||||||
| أرقام الأكسدة | +1, 0, -1 (أكاسيده قاعدية قوية) | ||||||||||||||||||||||||||||
| الكهرسلبية | 0.93 (مقياس باولنغ) | ||||||||||||||||||||||||||||
| طاقات التأين | الأول: 495.8 كيلوجول·مول−1 | ||||||||||||||||||||||||||||
| الثاني: 4562 كيلوجول·مول−1 | |||||||||||||||||||||||||||||
| التالت: 6910.3 كيلوجول·مول−1 | |||||||||||||||||||||||||||||
| نصف قطر ذري | 186 بيكومتر | ||||||||||||||||||||||||||||
| نصف قطر تساهمي | 9±166 بيكومتر | ||||||||||||||||||||||||||||
| نصف قطر فان دير فالس | 227 بيكومتر | ||||||||||||||||||||||||||||
| خواص تانيه | |||||||||||||||||||||||||||||
| البنية البلورية | مكعب مركزي الجسم | ||||||||||||||||||||||||||||
| المغناطيسية | مغناطيسية مسايرة | ||||||||||||||||||||||||||||
| مقاومة كهربائية | 47.7 نانوأوم·متر (20 °س) | ||||||||||||||||||||||||||||
| الناقلية الحرارية | 142 واط·متر−1·كلفن−1 (300 كلفن) | ||||||||||||||||||||||||||||
| التمدد الحراري | 71 ميكرومتر·متر−1·كلفن−1 (25 °س) | ||||||||||||||||||||||||||||
| سرعة الصوت (سلك رفيع) | 3200 متر/ثانية (20 °س) | ||||||||||||||||||||||||||||
| معامل يونغ | 10 غيغاباسكال | ||||||||||||||||||||||||||||
| معامل القص | 3.3 غيغاباسكال | ||||||||||||||||||||||||||||
| معامل الحجم | 6.3 غيغاباسكال | ||||||||||||||||||||||||||||
| صلادة موس | 0.5 | ||||||||||||||||||||||||||||
| صلادة برينل | 0.69 ميغاباسكال | ||||||||||||||||||||||||||||
| رقم الكاس | 7440-23-5 | ||||||||||||||||||||||||||||
| النظائر الأكثر ثباتاً | |||||||||||||||||||||||||||||
| المقالة الرئيسية: نظائر الصوديوم | |||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||
الصوديوم هو عنصر كيميائي رمزه Na (من النطرون) وعدده الذرّي 11. ينتمي العنصر فى الجدول الدوري لمجموعة الفلزّات القلوية كثاني عناصر المجموعة الأولى وضمن عناصر الدورة التالتة. الصوديوم فلزّ طري أبيض اللون، يتميّز بنشاطه الكيميائي الكبير لأنه بيتفاعل فى الهوا وبيتحرق بلهب أصفر، وشديد التفاعل مع الماء والرطوبة الجوّية، عشان كده بيتحفظ فى الزيوت أو مشتقّات النفط زي الكيروسين.[ْ 1]
مفيش صوديوم بشكل حرّ فى الطبيعة، وبيتم استخراجه من مركّباته. فى وفرة كبيرة تقريبا للصوديوم، لأنه سادس أكتر العناصر الكيميائية وفرة فى القشرة الأرضية، وموجود فى كتير من المعادن منها الفلدسبار والصوداليت والهاليت. بتتميز أملاح الصوديوم أنّ انحلاليتها كبيرة فى الماء، وأهمها ملح كلوريد الصوديوم، واللي بيعتبر المسبّب الرئيسي لملوحة مياه البحار. للصوديوم نظير واحد مستقر وهو 23Na.
للصوديوم دور حيويّ مهمّ، لأنه مصنّف ضمن العناصر الغذائية الأساسية للإنسان وللحيوانات وبعض النبات. فأيونات الصوديوم +Na هيا الكاتيونات الأساسية فى السائل خارج الخلايا، وليها دور أساسي فى تظبيط ضغط الدم والضغط التناضحي (الإسموزي) فى الجسم، بالإضافة لدوره فى نقل الإشارات العصبية (جهد الفعل).
التاريخ[تعديل]
الاكتشاف وأصل التسمية[تعديل]

على العكس من فلزّ الصوديوم الحرّ اللي تم اكتشافه لحد أوائل القرن ال 19 فإنّ مركّبات الصوديوم كانت معروفة ومتداولة من زمان، وخصوصا ملح الطعام المستخرج من البحر والبحيرات المالحة، وكمان من الأماكن الصخرية. وكان المصريون القدماء بيستخرجوا الأملاح من وادي النطرون، وعشان كده انتشرت كلمة نتر المصرية فى العهد القديم. وانتقلت الكلمة للغة الإغريقية علشان تكون νίτρον (نترون)، واللي استعملها العرب فبقت نطرون، ومنهم خدها الرومان وحوّروها علشان تكون nitrium (نتريوم).[5] وما زالت التسمية اللاتينية للعنصر Natrium وتحويرات منها مستخدمة فى عدّة لغات فى اللغة الألمانية ولغات منطقة إسكندنافيا وده حسب اقتراح من بيرسيليوس. بيتعقد البعض أنّ تسمية صوديوم بيعود أصلها للكلمة اللاتينية sodanum واللي معناها "علاج وجع الرأس"،[6] واللي متاخده من كلمة صداع بالعربي.[7] لكن الرأي ده ضعيف، والأغلب وصل اسم الصوديوم بكلمة صودا، والقادمة من اللاتينية soda اللي كانت بتشيرلنبات مزهر بينمو على الأراضي الملحية، زي نبات السويداء، واللي كان رماده (رماد الصودا) بيستخدم فى الغسيل، واللي من المرجح أن يكون اشتقاق كلمة صودا منه.[8]
اكتشف عنصر الصويوم لأوّل مرّة بشكله الحرّ عن طريق همفري ديفي سنة 1807 وده من التحليل الكهربائي لمصهور هيدروكسيد الصوديوم باستخدام عمود فولتي كمصدر كهربائي.[9][10] حسب اللي ورد فى سجلاّت الجمعية الملكية فى لندن، إنّ ديفي حصل فى عمليّته على ناتجين مختلفين: الناتج الأوّل الموجود فى الصودا سماه صوديوم، والتسمية دي المستخدمة للفلزّ باللغتين الإنجليزية والفرنسية، ومنها اتنقلت لأكتر من لغه تانيه، منها العربية. أمّا الفلزّ التاني المكتشف سماه بوتاسيوم. فى سنة 1809، و عشان توحيد التسمية اقترح العالم الألماني لودفيغ فيلهلم غيلبرت على ديفي استخدام Natronium (ناترونيوم) وKalium (كاليوم) أسمين للعنصرين اللي اكتشفوهم حديثاً.[11] نشر يونس ياكوب بيرسيليوس الرمز الكيميائي للصوديوم لأول مرة سنة 1814 وده ضمن مسعاه لتنظيم رموز العناصر الكيميائية،[12][13] واختار الرمز Na من كلمة Natrium فى اللاتينية الجديدة، واللي أخدها من كلمة نطرون العربية من المصرية القديمة، للإشارة للأملاح المعادن الطبيعية على شكل كربونات صوديوم مميّهة. كانت تسمية نطرون منتشرة فى أوروبا وكان السبب الإستخدام الكبير للمادّة على المستويين الصناعي والمنزلي.[14]
الخواص[تعديل]
يضفي الصوديوم لوناً أصفرلاللهب، وهذه ملاحظة تعودلسنة 1860، قام العالمان غوستاف روبرت كيرشهوف وروبرت بنسن بتدوين هذه الملاحظة فى منشورهم العلمي فى دورية Annalen der Physik.[15]
الوفرة الطبيعية[تعديل]

بسبب النشاط الكيميائي الكبير للعنصر، بقا أن مفيش صوديوم على شكله الحرّ على سطح الأرض، لكن بيدخل فى تركيب عدد كبير من المعادن، واللي بيتميز البعض منها بالانحلالية الكبيرة فى الماء زي الهاليت والنطرون. يعدّ ماء البحر واحد من أهم مصادر الصوديوم، كلّ ليتر منه بيكون موجود فيه حوالي11 غرام من أيونات الصوديوم،[16] وموجود فى المحيطات بحوالي 1.08××10قالب:Val/delimitnum ميليغرام فى كل ليتر.[17] أمّا فى أقلّ انحلالية زي مجموعة معادن الأمفيبول والزيوليتات. يعود ضعف الانحلالية لبعض المعادن الحاوية على الصوديوم زي الكريوليت والفلدسبارلالخاصّة البوليميرية للأنيونات، اللى تكون على شكل بولي سيليكات مثلاً فى الفلدسبار.
تحتوي القشرة الأرضية على الصوديوم بنسبة 2.36% من تركيبها، ممّا يجعله سادس اكتر العناصر وفرة فى القشرة الأرضية،[18] والخامس من ترتيب الفلزات بعد الألومنيوم والحديد والكالسيوم، وبنسبة مقاربة للمغنسيوم، لكن قبل البوتاسيوم.[19] من اكتر المعادن الحاوية على الصوديوم انتشاراً كلّ من الألبيت (NaAlSi3O8 فلدسبار الصوديوم) والأوليغوكلاس Na,Ca)Al(Si,Al)3O8)؛ كما فيه كمان بكمّيّات كبيرة نسبياً فى القباب الملحية على شكل هاليت (ملح الصخر). فيه الصوديوم فى الطبيعة كمان على شكل نترات الصوديوم (يعرف باسم ملح بيتر تشيلي) NaNO3، وهو واحد من المصادر الطبيعية القليلة لمعادن النترات، اللى تنتشر فى المناطق القاحلة مثل صحراء أتاكاما فى تشيلي؛ و ذلك تعدّ مكامن النطرون Na2CO3 · 10 H2O من المصادر المهمّة للصوديوم.
يحتلّ الصوديوم المرتبة 14 من وفرة العناصر فى الكون؛[20] وذلك بنسبة مقاربة للكالسيوم والنيكل. يتمّ التعرّف على الصوديوم فى الكتير من الأجرام السماوية (من ضمنها الشمس) كمان فى الوسط بين النجمي عن طريق الخطّ الطيفي D المميّز. رغم ارتفاع درجة حرارة تبخّره، إلاّ أنّ وفرته فى الغلاف الجوّي لكوكب عطارد مكّنت من كشفه بواسطة مسبار مارينر 10. كما تمكّن علماء الفلك وقت رصدهم مذنب هيل-بوب سنة 1997 من ملاحظة أنّ ذيل المذنب الممتدّ لحوالي 50 مليون كيلومتر يتكوّن من الصوديوم.[21]
الإنتاج والتحضير[تعديل]

يُنتج حوالي 100 ألف طنّ من الصوديوم الفلزّي سنويّاً، ويستخدم جلّ الإنتاج فى تطبيقات اختصاصية. يعود تاريخ إنتاج الصوديوم بشكل تجاريلأواخر القرن التسعتاشر،[22] وذلك بواسطة الاختزال الكربوحراري لمركّب كربونات الصوديوم (النطرون) عند درجات حرارة تفوق 1100 °س، وذلك كخطوة أولى فى عملية ديفيل لإنتاج الألومنيوم:[23][24][25]
إلّا أنّ هذه الطريقة لم تعد تستخدم للحصول على الصوديوم وذلك بعد تطوير عملية هول-هيرو لإنتاج الألومنيوم، اللى استغنت عن إنتاج الصوديوم كخطوة مرحلية. كما تمّ الاستغناء بسبب الكلفة المرتفعة عن عملية كاستنر، اللى طُوّرت سنة 1886، بالاعتماد على التحليل الكهربائي لهيدروكسيد الصوديوم.[26]
يُنتج الصوديوم حالياً بشكل تجاري من التحليل الكهربائي لمصهور كلوريد الصوديوم، اعتماداً على عملية حازت على براءة اختراع سنة 1924.[27][28] تتمّ العملية فى خلية داونز، اللى يمزج فيها ملح كلوريد الصوديوم مع كلوريد الكالسيوم (40% NaCl و60% CaCl2) للحصول على نظام أصهري علشان تخفيض نقطة الانصهار دون 700 °س، واختير الكالسيوم لأنه أقلّ كهرإيجابية من الصوديوم، فلا يترسّب على المهبط.[29] لإنتاج كيلوغرام واحد من الصوديوم يتمّ استهلاك 10 كيلوواط ساعي من التيّار وقت التحليل الكهربائي، وحوالي 12 كيلوواط ساعي فى العملية ككلّ.[30] تتكوّن خلايا التحليل الكهربائي الأسطوانية من مصعد من الغرافيت فى المنتصف، يحيط به مهبط من الحديد، و وجود قفص على شكل جرس لسحب أبخرة الكلور وقت العملية. يُجمّع الصوديوم المتشكّل على المهبط، ويُسحب بواسطة أنبوب صاعد من الخلية ومبرّد خارجها. يتشكّل الكالسيوم كمان كناتج ثانوي للعملية على شكل بلّورات، اللى يعاد تانىلمزيج الصهارة.
- تشكّل الصوديوم على المهبط
- تشكّل الكلور على المصعد
- التفاعل الإجمالي
نظراً للفاعلية الكيميائية الكبيرة لفلز الصوديوم، فهناك صعوبات تقنية ترافق تخزينه ونقله، ممّا أدّىلمحدودية انتشار إنتاجه. فالفلزّ لازم يحفظ إمّا فى جوّ من غاز خامل أو فى زيت معدني لامائي لتجنّب تشكّل طبقة سطحية من أكسيد الصوديوم أو فوق أكسيد الصوديوم.[31]
النظائر[تعديل]
هناك عشرون نظير مكتشف للصوديوم، تتراوح كتلها الذرّية من 18Naل33Na،[32] إلّا أنّه بس فيه نظير واحد مستقر، وهو صوديوم-23 23Na، بالتالي فالصوديوم عنصر أحادي النويدة. يتشكّل النظير 23Na فى عملية احتراق الكربون فى النجوم باندماج ذرّتي كربون، اللى يتطلّب درجات حرارة تتجاوز 600 ميغاكلفن، ونجم له ثلاث كتل شمسية على الأقلّ.[33]
للصوديوم نظيران مشعَّان ذَوا أصلٍ كوني، واللذان يتشكّلان من تشظية الأشعة الكونية وهما: صوديوم-22 22Na، اللى له عمر نصف مقداره 2.6 سنة، وصوديوم-24 24Na، اللى عمر النصف له يبلغ 15 ساعة. أمّا باقي نظائر الصوديوم فعمر النصف ليها أقلّ من دقيقة واحدة.[34] يُستخدم نظيرا الصوديوم 22Na و24Na فى الطب النووي كمواد اقتفاء.
اكتشف مصاوغان نووريان للصوديوم، أطولهما عمراً هو 24mNa (عمر النصف حوالي 20.2 ميلي ثانية. يؤدّي التعرّض للإشعاع النووي فى الحالات الحرجةلتحويل بعض من ذرّات النظير المستقرّ 23Na فى الدمّل24Na، ويمكن معرفة مدى جرعة التعرض للإشعاع النيوتروني بحساب نسبة تركيز النظير 24Naل23Na.[35]
الخواص الفيزيائية[تعديل]

يكون الصوديوم فى الظروف القياسية من الضغط ودرجة الحرارة على شكل فلزّ طري فضّي اللون، اللى يتّحد مع أكسجين الهواء ليشكّل طبقة رمادية اللون من الأكسيد. للحيلولة دون ذلك يتمّ فى العاده غمس الصوديوم الفلزي فى زيت معدني أو واحد من مشتقّات النفط، أو أن يحفظ فى جوّ من غاز خامل. ممكن قطع فلز الصوديوم بسهولة بالسكّين، فله قيمة صلادة تبلغ 0.5 حسب مقياس موس.[36] وهو ناقل جيّد للكهرباء وللحرارة، وذلك بسبب سهولة التخلّص من الإلكترون الوحيد الموجود فى غلاف التكافؤ، بالتالي يؤدّي ده التشكيل الإلكتروني للصوديوملضعف الرابطة الفلزية. بسبب قلّة الوزن الذرّي وكبر نصف قطرذرّة الصوديوم نسبياً، فإنّه يصنّف من الفلزّات الخفيفة، وهو تالت أقلّ الفلزّات كثافة (0.968 غ/سم3) بعد الليثيوم والبوتاسيوم، اللى هيا الوحيدة القادرة من بين الفلزات على العوم على سطح الماء.[37] يقع الصوديوم فى الكتير من خواصه بين الليثيوم والبوتاسيوم، فله نقطة انصهار (97.82 °س) أخفض من الليثيوم (180.54 °س)، إلّا أنّها أعلى من البوتاسيوم (63.6 °س)؛ كمان الأمر بالنسبة فى نقطة الغليان (883 °س) والحرارة النوعية.
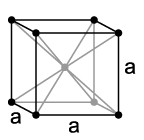
يتبلور الصوديوم كما هو الحال مع باقي الفلزّات القلوية وفق نظام بلوري مكعّب مركزي الجسم، له زمرة فراغية Im3m مع وجود وحدتي صيغة لكلّ وحدة خلية. عند درجات حرارة أدنى من 51 كلفن تتغيّر البنية البلّوريةلنظام تعبئة متراصّة سداسية، تبلغ قيمة ثابت الشبكة البلورية ليها a = 376 pm وc = 615 pm. تتغيّر خواص الصوديوم الظاهرية بشكل كبير عند ضغوط مرتفعة؛ فعند ضغط مقداره 1.5 ميغابار يتغيّر اللونلالأسود، وعند ضغط 1.9 ميغابار يصبح ذا لون أحمر شفاف، وعند 3 ميغابار يصبح الصوديوم ذا هيئة صلبة شفافة صافية، وتكون كل هذه المتآصلات عازلة وذات صفة إلكتريدية.[39]
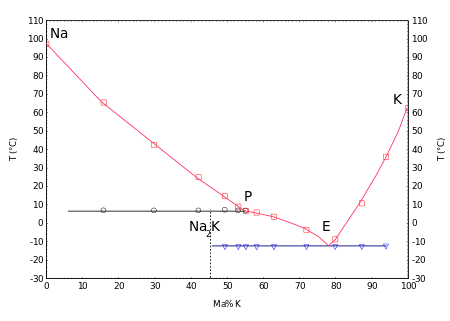
يتكوّن بخار الصوديوم، وهو ذو لون أصفرلأرجواني، من ذرّات فلزّية منفردة، ومن ثنائيات ليها الشكل Na2، والأخيرة تكون بنسبة 16% عند نقطة الغليان. يشكّل الصوديوم مع البوتاسيوم ضمن مجال عريض من التراكيز مزائج سائلة، يظهر المخطّط الطوري عند الدرجة 7 °س (وهي نقطة انصهار لا متطابقة Peritectic) التركيب Na2K، أمّا النقطة الأصهرية فهي عند − 12.6 °س، بوجود تركيز من البوتاسيوم مقداره 77% (كسر كتلي).[40]
الخواص الكيميائية[تعديل]
يظهر التشكيل الإلكتروني للصوديوم وجود 11 إلكترون فى الغلاف الإلكتروني، وهو يزيد بذلك بإلكترون واحد عن التشكيل الإلكتروني عالي الاستقرار للغاز النبيل المجاور وهو النيون. لده السبب، ولانخفاض قيمة طاقة التأيّن الأولى (495.8 كيلوجول/مول)، فإنّ ذرّات الصوديوم تميل لفقدان الإلكترون الأخير الموجود فى غلاف التكافؤ ولتشكيل كاتيون (أيون موجب الشحنة) +Na، وذلك بشكل اكبر من اكتساب إلكترون آخر ليصبح سالب الشحنة.[42] علشان كده فالصوديوم يميللتشكيل مركّبات أيونية، يكون للصوديوم فيها رقم تكافؤ مقداره +1 (طاقة التأيّن التانيه ليها قيمة مرتفعة جدّاً نسبيّاً: 4562 كيلوجول/مول).[43] يكون الصوديوم فى مركّباته الكيميائية مرتبطاً أيونياًلالأنيونات التانيه، ويصنّف أيون الصوديوم من أحماض لويس القاسية.[44]
إنّ الصوديوم اكتر نشاطاً كيميائياً من الليثيوم، لكنّه أقلّ من البوتاسيوم.[45] فهو يتفاعل بسهولة مع الكتير من العناصر وبعض المركّبات، ويكون تفاعله عنيفاً مع اللافلزّات مثل الكلور والكبريت، يترافق ذلك مع لهب أصفر. يعدّ الصوديوم الفلزّي من المختزلات القويّة، إذ يتطلّب اختزال أيونات الصوديوم جهداً مقداره −2.71 فولت،[46] رغم أنّ جهد الاختزال لكلّ من البوتاسيوم والليثيوم ذو قيم سالبة اكبر.[47]
يعدّ تفاعل الصوديوم مع الأكسجين حالة خاصة، إذ أنّ التفاعل بينهما مرهون بوجود الرطوبة، فبغياب الماء لا يتفاعل الصوديوم مع الأكسجين عند درجة حرارة الغرفة، وحتّى عند التسخين لا يتمّ التفاعل بشكل مباشر بينهما، كما ممكن صهر الصوديوم بجوّ من الأكسجين خالٍ من الماء بشكل تامّ دون حدوث تفاعل أيضاً. يتغيّر الأمر تماماً عند وجود الماء (الرطوبة)، فحينئذ يحترق الصوديوم بسهولة ليشكّل بيروكسيد الصوديوم:
يتفاعل الصوديوم مثل باقي الفلزات القلوية مع الماء بتفاعل عنيف ناشر للحرارة، يتشكّل هيدروكسيد الصوديوم وينطلق غاز الهيدروجين. بيّنت صور كاتشارة بسرعات فائقة أنّ تفاعل الفلزّات القلوية مع الماء يحدث بشكل أقرب ما يكون لانفجار كولوم.[48]
يتفاعل الصوديوم بشكل عنيف كمان مع الكحولات، لكن بشكل أخفّ من تفاعله مع الماء، ليشكّل الألكوكستات الموافقة، وغالباً مع انصهار الفلز بسبب حرارة التفاعل. يكون تفاعل الصوديوم عنيفاً كمان مع المذيبات العضوية الكلورية مثل ثنائي كلورو الميثان والكلوروفورم ورباعي كلوريد الكربون.
السبائك[تعديل]
يشكّل الصوديوم سبائك مع الكتير من الفلزّات مثل البوتاسيوم والكالسيوم والرصاص، و عناصر المجموعتين الحادية عشرة والثانية عشرة. يستطيع الصوديوم أن يشكّل مع البوتاسيوم سبيكة NaK، وتتراوح نسبة البوتاسيوم فى تركيبها من 40–90% هيا سائلة فى درجة الحرارة المعتدلة، وتتميّز بأنّ ليها خواص موصلية حرارية وكهربائية ممتازة. تعدّ سبائك صوديوم-كالسيوم منتجات ثانوية وقت إنتاج الصوديوم من عملية التحليل الكهربائي بوجود المزيج الملحي من NaCl-CaCl2، رغم أنّ الكالسيوم يمتزج بشكل جزئي بس مع الصوديوم.
في الحالة السائلة يمتزج الصوديوم مع الرصاص بشكل كامل. هناك الكتير من الوسائل اللى تمكّن من صنع سبائك صوديوم-رصاص، من بينها الصهر المشترك، وتانيه تتمثّل بترسيب الصوديوم كهربائياً على مهابط مصهورة مصنوعة من الرصاص. من الأمثلة على تركيبات سبائك صوديوم-رصاص كل من NaPb3 وNaPb وNa9Pb4 وNa5Pb2 وNa15Pb4.
من الممكن كمان الحصول على سبائك للصوديوم مع الذهب (NaAu2) والفضة (NaAg2). كذلك الأمر مع عناصر الزنك (NaZn13) والكادميوم (NaCd2) والزئبق، والعنصر الأخير يشكل ما يسمى ملغمة صوديوم: NaHg وNaHg4 وNaHg2 وNa3Hg2 وNa3Hg.[49]
المحاليل[تعديل]
يميل الصوديوملتشكيل مركّبات كيميائية منحلّة مثل أملاح الهاليدات والكبريتات والنترات والكربونات والكربوكسيلات. تكون الأنواع الكيميائية المائية الرئيسية على شكل المعقّد: +[Na(H2O)n] وقت عملية الإماهة، n = 4–8، مع العلم أنّ قيمة n = 6 حُدّدت بواسطة بيانات حيود الأشعة السينية والمحاكاة الحاسوبية.[50] للصوديوم انحلالية أقلّ فى المذيبات العضوية، فعلى سبيل المثال ينحلّ بس 0.35 غ/ل من كلوريد الصوديوم فى الإيثانول.[51]

كما هو الحال مع باقي الفلزات القلوية فإنّ الصوديوم ينحلّ فى الأمونيا وبعض الأمينات التانيه ليعطي محاليل ملوّنة غامقة، اللى يعود تلوّنهالالإلكترونات الحرّة اللى يمنحها الصوديوملالمحلول. بالتالي فالمحلول موصل للكهرباء، وعند تمديده يكون ذا مغناطيسية مسايرة.
يؤدّي تبخير هذه المحاليللترك طبقة رقيقة (فيلم) لامعة من الصوديوم الفلزّي. تحوي هذه المحاليل على معقدات تناسقية من النمط +(Na(NH3)6)، تُعاكَس الشحنة الموجبة بشكل مساوٍ عن طريق الإلكتريدات (الإلكترونات كأنيونات). ممكن استخدام الإيثرات التاجية، كحفّازات انتقال طوري؛[52] كما تسمح مركّبات كريبتاند بعزل هذه المعقّدات كمواد صلبة بلّورية، إذ أنّ الصوديوم يشكّل معقّدات معها كمان ومع ربيطات تانيه.[53] على سبيل المثال، فإنّ لمركّب إيثر 15-تاج-5 ألفة عالية تجاه الصوديوم، لأنّ حجم التجويف للمركّب يتراوح بين 1.7–2.2 أنغستروم (Å)، وهو مقدار كافٍ لينحشر أيون صوديوم داخله.[54][55] إنّ الكريبتاندات، مثلها مثل الإيثرات التاجية وحاملات الأيون التانيه، ذات ألفة عالية تجاه أيون الصوديوم، ب ممكن فى النهاية الحصول على مشتقّات من القلويدات −Na (ناتريد Natride: أنيون صوديوم)،[56] بواسطة إضافة مركّبات الكريبتاندلمحاليل من الصوديوم فى الأمونيا عن طريق تفاعل عدم تناسب.[57][58]
المركّبات الكيميائية[تعديل]
تعد المركّبات الكيميائية للصوديوم ذات أهمّيّة كبيرة، وذلك على مرّ التاريخ وخاصّة فى المجال التجاري والصناعي، كان ليها استخدام مركزي خاصّ فى صناعات مختلفة، منها صناعة الزجاج والورق والصابون والنسيج.
اللاعضوية[تعديل]
يعدّ كلوريد الصوديوم (ملح الطعام أو ملح المائدة، NaCl)، هو اكتر مركّبات الصوديوم اللاعضوية شيوعاً، وذلك مع كربونات الصوديوم (رماد الصودا، Na2CO3) وبيكربونات الصوديوم (صودا الخبز، NaHCO3) وهيدروكسيد الصوديوم (الصودا الكاوية، NaOH) ونترات الصوديوم (نتر الصودا، NaNO3)، كمان أملاح فوسفات الصوديوم الثنائية والثلاثية، و ثيوكبريتات الصوديوم (Na2S2O3·5H2O) والبورق (Na2B4O7·10H2O).
- الهاليدات
أشهر هاليدات الصوديوم هو مركب كلوريد الصوديوم NaCl المتوفّر بكثرة، ويعدّ المصدر الأساسي للحصول على الصوديوم فى الطبيعة. أمّا باقي الهاليدات فهي مركّبات ثابتة ومعروفة، وهي: فلوريد الصوديوم NaF، وبروميد الصوديوم NaBr، ويوديد الصوديوم NaI.

- الهيدريدات
للصوديوم مركّبين ينتميانلالهيدريدات وهما هيدريد الصوديوم NaH، وبورهيدريد الصوديوم NaBH4، واللذان يستخدمان فى الاصطناع العضوي كمختزلات.
- المركّبات الأكسجينية
يرتبط الصوديوم مع الأكسجين ليشكّل عدّة أكاسيد أشهرها: أكسيد الصوديوم Na2O، وبيروكسيد الصوديوم Na2O2، وفوق أكسيد الصوديوم NaO2. تستخدم أكاسيد الصوديوم المختلفة فى صناعة الزجاج والورق والنسيج. يعدّ هيدروكسيد الصوديوم NaOH من القلويات الشائعة، يستخدم محلوله بشكل كبير فى الصناعة.
- المركّبات الكبريتية
يعطي الصوديوم مع كبريتيد الهيدروجين ملحين وهما: كبريتيد الصوديوم Na2S وبيكبريتيد الصوديوم NaHS، واللذان يستخدمان فى تعدين الفلزّات الثقيلة. يستخدم كبريتات الصوديوم Na2SO4 فى صناعة الورق، أمّا بيكبريتات الصوديوم فيستخدم فى منتجات التنظيف. من مركّبات الصوديوم الكبريتية كمان مركب ثيوكبريتات الصوديوم اللى يستخدم فى التصوير الضوئي.
- أملاح تانيه
يصنّف مركبا كربونات الصوديوم Na2CO3 وبيكربونات الصوديوم NaHCO3 على أنّهما أملاح صوديومية لحمض الكربونيك، هيا واسعة الانتشار والاستخدام على الصعيدين المنزلي والصناعي، وذلك و نترات الصوديوم NaNO3 ومركّبات فوسفات الصوديوم المختلفة.
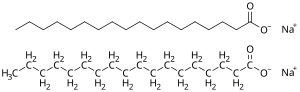
إنّ أغلب منتجات الصابون هيا أملاح صوديوم للأحماض الدهنية، تمتاز هذه المنتجات بأنّ ليها قوام صلب متماسك، وذلك بالمقارنة مع نظيراتها من أملاح البوتاسيوم، اللى تدخل فى تركيب الصابون السائل.[59]
العضوية[تعديل]
جرى تحضير الكتير من مركّبات الصوديوم العضوية، وبسبب استقطاب الرابطة الكيميائية بين C-Na فإنّ هذه المركّبات تعدّ كمصدر للكربانيونات. من بين هذه المركّبات حلقي بنتاديينيد الصوديوم NaC5H5 وتريتيل الصوديوم (C6H5)3CNa)).[60]
بسبب كبر حجم وضعف القوة المستقطبة للكاتيون +Na فإنّه يستطيع أن يثبّت الأنيونات العطرية الجذرية الكبيرة القابلة للاستقطاب، مثلما هو الحال فى نفثالينيد الصوديوم −[•Na+[C10H8، وهو مختزل قويّ جدّاً.[61]
الكشف عن الصوديوم[تعديل]
اختبار اللهب[تعديل]

عند إجراء اختبار اللهب يعطي الصوديوم ومركّباته لوناً أصفر مميّز،[62] وذلك بسبب أنّ الإلكترونات فى المدار الذري 3s تتهيّج وتثار بسبب امتصاص الحرارة وتقفزلالمدار 3p، وعند عودتهالالمدار 3s تصدر طاقة على شكل فوتون له طول موجة عند 589.3 نانومتر، ويرمز له الخطّ D فى خطوط فراونهوفر. يؤدّي التآثر المغزلي المداري للإلكتروناتلانفصام الخط Dلخطّين D1 وD2، كما تسبّب البنى فائقة الدقة فى المداراتلالحصول على خطوط ضعيفة تانيه.[63]
الكيمياء التحليلية[تعديل]
من النادر حدوث عملية ترسيب لأملاح الصوديوم، لأنّ ليها ألفة كيميائية عالية تجاه الماء، باستمدح ملح بزموتات الصوديوم (NaBiO3).[64] كما أنّه من الممكن إجراء ترسيب للصوديوم باستخدام ملح مزدوج صوديومي من الكبريتات والبزموت 3Na2SO4*2Bi2(SO4)3*2H2O.[65]
يمكن تحديد المحتوى الصوديومي فى المواد بالمعالجة مع كمّيّة فائضة من أسيتات يورانيل الزنك؛ يترسّب سداسي الهيدرات UO2)2ZnNa(CH3CO2)·6H2O) ويحدد وزنه. لا يتداخل السيزيوم والروبيديوم فى تفاعل الكشف ده، لكن التداخلات تحدث مع عنصري البوتاسيوم والليثيوم.[66] كما ممكن أن يتمّ الكشف بالترسيب باستخدام أسيتات يورانيل الصوديوم والمغنسيوم [67] يعطي راسب أصفر من NaMg(UO2)3(CH3COO)9·9 H2O؛ أو باستخدام سداسي هيدروكسي إثمدات الصوديوم [Na[Sb(OH)6 اللى يعطي راسب عديم اللون.[68]
تحدّد التراكيز الضئيلة من الصوديوم بواسطة مطيافية الامتصاص الذري،[69] أو بإجراء معايرة بمقياس الجهد باستخدام أقطاب انتقائية لأيونات الصوديوم.[70]
الدور الحيوي[تعديل]
للصوديوم دور حيويّ مهمّ فى جسم الإنسان، فهو من العناصر الغذائية الضرورية اللى تلعب أدواراً متنوّعة فى الكتير من العمليّات الفسيولوجية مثل ضغط الدم وحموضة (pH) الوسط فى الجسم، و تنظيم التوازن المائي داخل وخارج الخلايا. فيه الصوديوم فى الجسم على شكل أيونات (+Na)، هيا من الكهارل (الإلكتروليتات) المهمّة فى أداء العصبونات؛ هيا السائدة فى السائل خارج الخلوي،[71] تقوم بضبط الضغط التناضحي (الإسموزي) بين الخلايا وخارجها عن طريق مضخّة الصوديوم والبوتاسيوم (Na+/K+-ATPase)، وهو إنزيم مسؤول عن النقل الفعّال للأيونات عبر القنوات المخصّصة.[72]
- الضبط
يقوم نظام الرينين-أنجيوتنسين بتنظيم كمّيّة السوائل وبالتالي تركيز الصوديوم فى الجسم، وتلعب الكلية الدور الرئيسي فى ذلك.[73] عند انخفاض ضغط الدم وتركيز الصوديوم، فإنّ الجسم يستجيب بإفراز الرينين، اللى بدوره يسبّب إفراز الألدوستيرون والأنجيوتنسين،لأن يصبح تركيز الصوديوم طبيعياً، فينخفض إفراز الرينين.[74] كما يلعب هرمون فازوبرسين والببتيد الأذيني المدرّ للصوديوم دوراً فى عملية التنظيم هذه.[75]
يقع تركيز الصوديوم الطبيعي فى مصل الدم بين حوالي 135–145 ميلي مول/ليتر (mmol/l). توصف الحالات فى الطبّ اللى ترافق حدوث ارتفاع غير عادي من الصوديوم فى الدم باسم فرط صوديوم الدم، اللى يترافق بانكماش الخلايا؛ بالمقابل فإنّ الانخفاض غير العادي يسمى نقص صوديوم الدم، اللى يترافق بازدياد حجم الخلايا. قد يعود سبب هذه الحالات المرضيةلعوامل وراثية أو تقدّم العمر أو الحالات المطوّلة من الإقياء أو الإسهال.[76]
- التوزيع فى الخلايا
لا تتوزّع أيونات الصوديوم +Na فى أجسام الكائنات الحية بانتظام، فهي متفاوتة بين داخل الخلايا وخارجها، ممّا يؤدّي فى النهايةلالتأثير على الجهد الغشائي فيها. يعدّ الجهد الغشائي وتدرّج تراكيز الأيونات من العوامل المؤثّرة على أداء الخلايا، وفي ده السياق تلعب مضخّة الصوديوم والبوتاسيوم دوراً مهمّاً فى ذلك، تُدخل البوتاسيوم وتُخرج الصوديوم بعملية مستهلكة للطاقة.[77]
- الدور العصبي
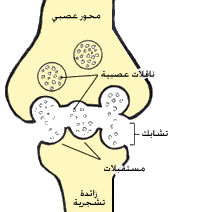
لأيونات الصوديوم +Na دور مهمّ فى تشكيل ونقل الإثارات الحسّية فى العصبونات، فعند التشابك العصبي (وكذلك عند المشابك العصبية العضلية أيضاً) توجد هناك مستقبلات بروتينية عبر غشائية محدّدة، اللى بعد تحفيزها من النواقل العصبية المفرَزة من الخليّة العصبية المجاورة تقوم بفتح المجال لعبور أيونات الصوديوم. عند مرور تيّار من أيونات الصوديوم يحدث هناك تغيّر موضعي فى الجهد الغشائي للخليّة، يصبح الكمون الداخلي أقل سلبيّة من الكمون الخارجي، ويحدث ما يسمى بعملية إزالة الاستقطاب، اللى تتكرّر على طول المحور العصبي بفتح وإغلاق للقنوات الأيونية، ممّا يؤدّيلحدوث جهد الفعل.
- المصادر والكميّة
يمثّل كلوريد الصوديوم المصدر الرئيسي للصوديوم فى النظام الغذائي للإنسان، يستخدم كملح للطعام، و استخداماته المختلفة فى وسائل حفظ المأكولات المختلفة مثل التخليل والتقديد، كما يستخدم بشكل كبير فى المأكولات سهلة التحضير.[78][ْ 2]
بالإضافةلالمصادر الطبيعية للصوديوم، فإنّ الجسم يحصل عليه من الإضافات الغذائية مثل أحادي غلوتامات الصوديوم (E621) ونتريت الصوديوم (E250) وبنزوات الصوديوم (E211) وصوديوم السكارين وبيكربونات الصوديوم (صودا الخَبْز - ذرور الخبز).[79]
في جسم إنسان متوسّط وزنه 70 كغ فيه حوالي 100 غ من أيونات الصوديوم.[80] إنّ الحدّ الأدنى المتطلّب فسيولوجياً من الصوديوم هو 500 ميليغرام فى اليوم وسطيّاً،[81] وحدّدته الجمعية الألمانية للتغذية بمقدار 550 مغ/اليوم للبالغين، وحوالي 460 مغ/اليوم للأطفال بين عمر السابعة والعاشرة.[82] هناك توصيات من عدّة منظّمات لضبط الكمّيّة الأعظمية من الصوديوم فى الغذاء، حدّدته منظّمة الصحّة العالمية (WHO) بمقدار 2 غ/اليوم،[83] فى حين أنّ الأكاديمية الوطنية الأمريكية للطبّ حدّدت الكمّيّة الغذائية المرجعية (DRI) من الصوديوم بمقدار 2.3 غ يومياً كحدّ أعظمي.[84] بيّنت الدراسات أنّ تقليل كمّيّات الصوديوم المتناولةل2 غ فى اليوم يسهم فى تخفيض ضغط الدم بمقدار 2 - 4 ميليمتر زئبقي؛[85] ممّا يؤدّيلنسبة حالات أقل من ارتفاع ضغط الدم تتراوح ما بين 9 - 17 %؛ مع العلم أنّ ارتفاع ضغط الدم يسبّب 7.6 مليون حالة وفاة مبكّرة سنويّاً حول العالم.[86] بملاحظة أنّ ملح الطعام يحوي على 39.3% من تركيبه على صوديوم،[87] بالتالي فإنّ الحدّ الأعظمي المذكور آنفاً من 2.3 غ صوديوم يكافئ حوالي 6 غ من الملح فى اليوم (ملعقة شاي تقريباً).[88] مع العلم أنّ جمعية القلب الأمريكية [89] توصي بأن تكون كمّيّة الصوديوم فى الغذاء حوالي 1.5 غ يومياً؛ هيا الكمّيّة الموصى بيها من إدارة الغذاء والدواء الأمريكية (FDA) للمصابين بفرط الضغط أو أعراضه. هناك الكثير ممّن يتناولون كمّيّات من الصوديوم اكبر بكثير من اللى يحتاجون ليها،[ْ 3] ممّا يعرّضهم للخطر، لذالازممراقبة تركيز الصوديوم بإجراء ما يسمى اختبار الصوديوم لعينة من الدم،[ْ 4] أو من البول؛[90] إذ بيّنت دراسة أنّ المستويات المرتفعة من الصوديوم فى البول (حوالي 7 غ فى اليوم) عند المصابين بارتفاع الضغط ممكن أن يعرّضهم لأزمات قلبية ويرفع من نسبة حدوث الوفاة.[91]
- النباتات
في النباتات ذات التمثيل الضوئي رباعي الكربون فإنّ الصوديوم يعدّ من المغذيات الأصغرية اللى ليها دور ثانوي لكن مهمّ؛ تسهم فى عملية الاستقلاب، وخاصّة فى إعادة توليد فوسفوإينول حمض البيروفيك واصطناع الكلوروفيل.[92] كما يحلّ الصوديوم مكان البوتاسيوم فى بعض النباتات التانيه، كما هو الحال مع النباتات الملحية، يقوم بالإبقاء على ضغط الامتلاء ويساعد فى فتح وإغلاق الثغور النباتية،[93]
يسبّب ارتفاع تركيز الصوديوم فى التربةلالحدّ والتقليل من استهلاك الماء فى النبات عبر جهد الماء، اللى يؤدّي بدورهلالذبول.[94][95] كما أنّ ارتفاع تركيز الصوديوم فى السيتوبلازم ممكن أن يسبّب تثبيط الإنزيمات، اللى بدوره يؤدّيلالنخر وشحوب الأوراق.[96] كردّ فعل، تقوم بعض النباتات بتطوير آلية للحدّ من استجلاب الصوديوم فى الجذور النباتية، أو بتخزينه فى الفجوات العصارية، أو بالحدّ من نقل الملح من الجذورلالأوراق.[97] تسمّى هذه النباتات اللى تقوم بذلك أنّها كارهة للصوديوم، ومن أمثلتها الفاصولياء الشائعة والذرة.
الاستخدامات[تعديل]

هناك طلب كبير على مركّبات الصوديوم فى الصناعة، وخاصّة أملاح الكلوريد والهيدروكسيد والكربونات لاستخداماتها المتنوّعة، وذلك بشكل اكبر من الطلب على الصوديوم الفلزّي بحدّ ذاته. يستخدم الصوديوم مع البوتاسيوم على شكل أيون فى الكتير من الأدوية والمستحضرات الصيدلانية لتحسين التوافر الحيوي؛ رغم أفضليّة أيون البوتاسيوم فى حالات عدّة، إلّا أنّ الصوديوم هو اللى يتم اختياره لانخفاض سعره ووزنه الذرّي.[98] يستخدم الصوديوم بشكل مباشر فى تحضير مركّبات الصوديوم قليلة الانتشار فى الطبيعة، اللى لا ممكن تحضيرها من كلوريد الصوديوم، وذات التطبيقات البالخصوص مثل بيروكسيد الصوديوم وأميد الصوديوم وسيانيد الصوديوم وهيدريد الصوديوم وبورهيدريد الصوديوم وأزيد الصوديوم؛ و تحضير صبغة النيلة ومركّب ثلاثي فينيل الفوسفين.
كان الصوديوم مستخدماً لوقت طويل فى إنتاج رباعي إيثيل الرصاص من كلورو الإيثان، اللى كان يمزج فى الماضي بكثرة مع وقود السيارات كمانع للخبط فى محركات الاحتراق الداخلي؛ قبل ما يمنع لأسباب صحّية وبيئية فى أغلب دول العالم، ممّا أدّىلانخفاض إنتاج الصوديوم عالميّاً من سبعينات القرن العشرين.[99]
التحفيز[تعديل]
يستخدم الصوديوم فى تحفيز بلمرة 3،1-بوتاديين والإيزوبرين، وفي إنتاج المطّاط الاصطناعي.[100] كان يطلق على المطّاط الاصطناعي المنتَج باستخدام الصوديوم كحفّاز اسم بونا Buna، وكان من أوائل أنواع المطّاط الاصطناعي المنتج فى العالم.[101]
التبريد[تعديل]
يستخدم الصوديوم السائل فى تبريد المفاعلات النووية لقدرته العالية على نقل الحرارة.[ْ 5] فللصوديوم ناقلية حرارية تبلغ 140 واط/م.كلفن، هيا قيمة تفوق اللى للفولاذ (الصلب، 58 واط/م.كلفن)، كما أنّه سهل الانصهار وذو نقطة غليان مرتفعة نسبيّاً ممّا يمكّن من العمل فى المفاعلات تحت ضغوط عادية غير مرتفعة. كما أنّ له مقطع تصادم صغير مع النيوترونات،[102] ممّا يجعله جيّداً للاستخدام كمادة تبريد للمفاعلات النووية مثل مفاعل الاستنسال السريع،[103] اللى لا يستخدم الماء للتبريد فيها لتجنّب كبح النيوترونات.[104]
لكن من مساوئ استخدام الصوديوم فى تبريد المفاعلات النووية هو عدم شفافيّته (اعتامه)، ممّا يعيق إصلاح الأعطال بصرياً، و خطر وقوع حوادث انفجارية.[105] كما ممكن أن يتكوّن النظير صوديوم-24 عبر تنشيط النيوترون وقت التشغيل، ممّا قد يشكّل خطر إشعاع بسيط؛ فالنشاط الإشعاعي يتوقّف بعد عدّة أيام من إزالته من المفاعل.[106] لما تكون هناك الحاجة لإيقاف وإعادة تشغيل المفاعل لعدّة مرات، فإنّه من الاحسن استخدام سبيكة صوديوم-بوتاسيوم (NaK) للتبريد، إذ أنّها سائلة عند درجة حرارة الغرفة، بالتالي لا تتصلّب مادة التبريد فى الأنابيب؛[107] لكن بالمقابل يُخشى من تلقائية اشتعال البوتاسيوم، ممّا يستدعي اتخاذ إجراءات احترازية إضافية.[108]
من التطبيقات الحرارية للصوديوم كمان استخدامه فى الصمّامات القَفَّازة فى محرّكات الاحتراق الداخلي عالية الأداء؛ إذ أنّ ساق الصمام تكون مملوءةً جزئياً بالصوديوم وتعمل كأنبوب حراري لتبريد الصمّام.[109]
الإنارة[تعديل]
لإنارة الشوارع يستخدم أحياناً مصابيح بخار الصوديوم، اللى تتميّز بلونها الأصفر البرتقالي، اللى يتشكّل عند تعريض بخار الصوديوملتفريغ كهربائي.[110]
الاختزال[تعديل]
يتميّز الصوديوم بأنّه من المختزلات القويّة، و علشان كده يستخدم فى تعدين بعض الفلزّات اللى لا ممكن اختزالها بالكربون مثل التيتانيوم والزركونيوم والتانتالوم واليورانيوم والألومنيوم والمغنسيوم، لأنّ هذه الفلزات تشكّل كربيدات ثابتة حرارياً صعبة التفكك. كما ممكن استخدام البوتاسيوم لده الغرض أيضاً.
في المجال المخبري يستخدم الصوديوم كمختزل مهمّ فى الاصطناع العضوي،[111] مثل اختزال بيرتش وتفاعل ازدواج البيناكول.[112] يستخدم ناتج إذابة الصوديوم فى الأمونيا لاختزال الألكايناتلألكينات المفروقة (ترانس).[113][114]
التجفيف[تعديل]
بسبب القابلية المرتفعة للتفاعل لحد مع آثار من الماء، ممكن أن يستخدم سلك مضغوط من الصوديوم كمجفّف للمذيبات العضوية مثل ثنائي إيثيل الإيثر والتولوين. بالمقابل لا ممكن استخدام هذه الطريقة لتجفيف الكحولات أو المذيبات الهالوجينية (مثل ثنائي كلورو الميثان) لأنّ الصوديوم يتفاعل معها. ممكن استخدام NaK لغرض التجفيف أيضاً، تبدي ميّزات نوعية فى ده المجال. يعطي ناتج عملية التجفيف بالصوديوم (أو NaK) لوناً شديد الزرقة مع مركّب بنزوفينون.[115]
احتياطات الأمان[تعديل]
عند التماس مع الماء يشكّل الصوديوم غاز الهيدروجين القابل للاشتعال، و محلول هيدروكسيد الصوديوم الأكّال.[116] بالتالي فإن ابتلاع الصوديوم وتماسّه مع الجلد أو العين أو الأغشية المخاطية يسبّب حروقاً شديدة.[117][118] ينفجر الصوديوم بشكل تلقائي بوجود المؤكسدات.[119]
إنّ مطافئ الحريق ذات الأساس المائي غير مناسبة لإطفاء حرائق الصوديوم، فهي تعمل بالعكس على تسريعها، كما ينبغي تجنّب استعمال مطافئ ذات أساس من ثنائي أكسيد الكربون وبرومو كلورو ثنائي فلورو الميثان (هالون 1211) أيضاً. يستخدم لإطفاء حرائق الفلزّات مطافئ من الصنف D (بودرة جافّة)، اللى يعتمد بعضها مثلاً (Lith-X) على مسحوق من الغرافيت والرمل ومثبّط لهب فوسفاتي عضوي.[120]
تُكافَح حرائق الصوديوم فى المفاعلات النووية بعزل الصوديوم عن الأكسجين بإحاطة أنابيب الصوديوم بغاز خامل.[121] أمّا حرائق الصوديوم ذات النمط البِرَكي فتكافَح بأسلوب مختلف يعتمد على تجميع الصوديوم المتسرّب وسَوقِهلخزّانات استرجاع لعزله عن الأكسجين.
المراجع[تعديل]
باللغة العربية[تعديل]
- ↑ أ ب http://www.rsc.org/periodic-table/element/11/sodium — تاريخ الاطلاع: 28 يوليه 2018
- ↑ المؤلف: Michael E. Wieser ، Tyler B. Coplen و Michael Wieser — العنوان : Atomic weights of the elements 2009 (IUPAC Technical Report) — المجلد: 83 — الصفحة: 359–396 — العدد: 2 — نشر في: Pure and Applied Chemistry — https://dx.doi.org/10.1351/PAC-REP-10-09-14
- ↑ https://www.cns11643.gov.tw/wordView.jsp?ID=90716 — تاريخ الاطلاع: 13 يوليه 2019
- ↑ Endt، P. M. ENDT, ,1 (1990) (12/1990). "Energy levels of A = 21-44 nuclei (VII)". Nuclear Physics A. 521: 1. doi:10.1016/0375-9474(90)90598-G. تحقق من التاريخ في:
|date=(مساعدة) - ↑ Mineralienatlas: Natrium.واي باك مشين Archived 2017-11-11 at the Wayback Machine
- ↑ "soda in Online Etymology Dictionary". 2001-2016 Douglas Harper.
{{cite web}}: Empty citation (help)الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة) - ↑ Newton، David E. (1999). المحرر: Baker، Lawrence W. Chemical Elements. ISBN 978-0-7876-2847-5. OCLC 39778687.Baker, Lawrence W. (ed.). ISBN 978-0-7876-2847-5. OCLC 39778687.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|عنوان=ignored (help)الوسيط|الأول=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ English Words That Are Of Arabic Etymological Ancestry: Note #186, Soda
- ↑ . doi:10.1098/rstl.1808.0001.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|مسار=ignored (help) - ↑ . Bibcode:1932JChEd...9.1035W. doi:10.1021/ed009p1035.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|العدد=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|عنوان=ignored (help) - ↑ Humphry Davy (1809) "Ueber einige neue Erscheinungen chemischer Veränderungen, welche durch die Electricität bewirkt werden; insbesondere über die Zersetzung der feuerbeständigen Alkalien, die Darstellung der neuen Körper, welche ihre Basen ausmachen, und die Natur der Alkalien überhaupt" (On some new phenomena of chemical changes that are achieved by electricity; particularly the decomposition of flame-resistant alkalis [i.e., alkalies that cannot be reduced to their base metals by flames], the preparation of new substances that constitute their [metallic] bases, and the nature of alkalies generally), Annalen der Physik, 31 (2) : 113–175 ; see footnote p. 157. From p. 157: "In unserer deutschen Nomenclatur würde ich die Namen Kalium und Natronium vorschlagen, wenn man nicht lieber bei den von Herrn Erman gebrauchten und von mehreren angenommenen Benennungen Kali-Metalloid and Natron-Metalloid, bis zur völligen Aufklärung der chemischen Natur dieser räthzelhaften Körper bleiben will. Oder vielleicht findet man es noch zweckmässiger fürs Erste zwei Klassen zu machen, Metalle und Metalloide, und in die letztere Kalium und Natronium zu setzen. — Gilbert." (حسب قواعد التسمية الألمانية، أقترح عليك استخدام الاسمين Kalium (كاليوم) وNatronium (ناترونيوم)، وذلك لإيقاف استخدام مصطلحات Kali-metalloid' (شبه فلز القلي) وNatron-metalloid (شبه فلز النطرون) المستخدمة على ايد السيد Erman (إرمان)، اللى لقت قبولاً من الكتير من الأطراف، حتّى يتّضح بشكل كامل الماهية والطبيعة الكيميائية لهذه المواد المحيّرة. أو ربّما من الاحسن فى الوقت الحاضر إنشاء صنفين من المواد: فلزّات وشبه فلزّات، مع وضع Kalium (كاليوم) وNatronium (ناترونيوم) فى الصنف الأخير. Archived 2016-12-07 at the Wayback Machineواي باك مشينArchived 2016-12-07 at the Wayback Machine
- ↑ J. Jacob Berzelius, Försök, att, genom användandet af den electrokemiska theorien och de kemiska proportionerna, grundlägga ett rent vettenskapligt system för mineralogien [Attempt, by the use of electrochemical theory and chemical proportions, to found a pure scientific system for mineralogy] (Stockholm, Sweden: A. Gadelius, 1814), p. 87.
- ↑ van der Krogt، Peter. "Elementymology & Elements Multidict". اطلع عليه بتاريخ 08 يونيه 2007.
{{cite web}}: Empty citation (help)الوسيط|الأول=تم تجاهله (مساعدة); الوسيط|تاريخ الوصول=تم تجاهله (مساعدة); الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة) - ↑ "Natron as a flux in the early vitreous materials industry: sources, beginnings and reasons for decline". Andrew Shortland, Lukas Schachner, Ian Freestone, and Michael Tite.
{{cite web}}: Empty citation (help)الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|العمل=تم تجاهله (مساعدة) - ↑ . Bibcode:1860AnP...186..161K. doi:10.1002/andp.18601860602.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|العدد=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|عنوان=ignored (help) - ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. de Gruyter, Berlin 2007, ((ردمك 978-3-11-017770-1), S. 695.
- ↑ Lide، David R. (2003-06-19). CRC Handbook of Chemistry and Physics, 84th Edition. CRC Handbook (باللغة الإنجليزية). CRC Press. 14: Abundance of Elements in the Earth's Crust and in the Sea. ISBN 978-0-8493-0484-2.. CRC Handbook. 14: Abundance of Elements in the Earth's Crust and in the Sea. ISBN 978-0-8493-0484-2.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|لغة=ignored (help); Unknown parameter|مسار=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الأول=تم تجاهله (مساعدة); الوسيط|اللغة=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة). CRC Handbook. 14: Abundance of Elements in the Earth's Crust and in the Sea. ISBN 978-0-8493-0484-2.{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|لغة=ignored (help); Unknown parameter|مسار=ignored (help); Unknown parameter|ناشر=ignored (help) - ↑ K. H. Wedepohl: The composition of the continental crust. In: Geochimica et Cosmochimica Acta. 59, 7, 1995, S. 1217–1232; doi:10.1016/0016-7037(95)00038-2.
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 0-08-037941-9, p. 69
- ↑ A. G. W. Cameron: Abundances of the elements in the solar system. In: Space Science Reviews. 15, 1970, S. 121–146; doi:10.1007/BF00172440.
- ↑ . arXiv:astro-ph/9710022. Bibcode:1997ApJ...490L.199C. doi:10.1086/311040.
{{cite journal}}: Cite journal requires|journal=(help); Invalid|display-authors=8(help); Missing or empty|title=(help); Unknown parameter|العدد=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|سنة=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|عنوان=ignored (help)CS1 maint: display-authors - ↑ B. Pearson (المحرر). Speciality Chemicals: Innovations in industrial synthesis and applications (الطبعة illustrated). Springer Science & Business Media, 1991. صفحة 260. ISBN 1-85166-646-X.. ISBN 1-85166-646-X.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|صفحة=ignored (help); Unknown parameter|طبعة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|محرر=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|المحرر=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الطبعة=تم تجاهله (مساعدة); الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ Eggeman، Tim؛ Updated By Staff (2007). "Sodium and Sodium Alloys". Kirk-Othmer Encyclopedia of Chemical Technology. John Wiley & Sons. ISBN 0-471-23896-1. doi:10.1002/0471238961.1915040912051311.a01.pub3."Sodium and Sodium Alloys". doi:10.1002/0471238961.1915040912051311.a01.pub3. ISBN 0-471-23896-1.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير1=ignored (help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأول1=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الأول1=تم تجاهله (مساعدة); الوسيط|الأخير1=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الأخير2=تم تجاهله (مساعدة) - ↑ . doi:10.2307/27757153. JSTOR 27757153.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|عنوان=ignored (help) - ↑ . Bibcode:1990JChEd..67.1046B. doi:10.1021/ed067p1046.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|العدد=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|وصلة=ignored (help) - ↑ Mark Anthony Benvenuto. Industrial Chemistry: For Advanced Students (الطبعة illustrated). Walter de Gruyter GmbH & Co KG, 2015. ISBN 3-11-038339-X.. ISBN 3-11-038339-X.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|طبعة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|مؤلف=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الطبعة=تم تجاهله (مساعدة); الوسيط|المؤلف=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ Pauling, Linus, General Chemistry, 1970 ed., Dover Publications
- ↑ "Los Alamos National Laboratory – Sodium". اطلع عليه بتاريخ 08 يونيه 2007.
{{cite web}}: Empty citation (help)الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|تاريخ الوصول=تم تجاهله (مساعدة) - ↑ Sodium Metal from France. DIANE Publishing. ISBN 1-4578-1780-2.. ISBN 1-4578-1780-2.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة) - ↑ Zusammenfassung über Alkalimetalle von wiley-vch(PDF; 423 kB).واي باك مشين Archived 2016-03-04 at the Wayback Machine
- ↑ Stanley Nusim (المحرر). Active Pharmaceutical Ingredients: Development, Manufacturing, and Regulation, Second Edition (الطبعة 2, illustrated, revised). CRC Press, 2016. صفحة 303. ISBN 1-4398-0339-0.. ISBN 1-4398-0339-0.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|صفحة=ignored (help); Unknown parameter|طبعة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|محرر=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|المحرر=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|الطبعة=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ G. Audi, O. Bersillon, J. Blachot, A. H. Wapstra: The Nubase evaluation of nuclear and decay properties Archived 2011-07-20 at the Wayback Machine. (PDF; 1 MB)
- ↑ . Bibcode:1987SvAL...13..214D.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|عنوان=ignored (help) - ↑ . Bibcode:2003NuPhA.729....3A. doi:10.1016/j.nuclphysa.2003.11.001.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير3=ignored (help); Unknown parameter|الأخير4=ignored (help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول3=ignored (help); Unknown parameter|الأول4=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|عنوان=ignored (help) - ↑ . doi:10.1097/00004032-196208000-00005. PMID 14496815.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|العدد=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|عنوان=ignored (help) - ↑ Natrium bei webelements.com, physikalische Eigenschaften.واي باك مشين Archived 2017-11-25 at the Wayback Machine
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 0-08-037941-9, p. 75
- ↑ K. Schubert: Ein Modell für die Kristallstrukturen der chemischen Elemente. In: Acta Crystallographica. B30, 1974, S. 193–204; doi:10.1107/S0567740874002469.
- ↑ . arXiv:1003.0540. Bibcode:2010PhRvL.104u6404G. doi:10.1103/PhysRevLett.104.216404. PMID 20867123.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير3=ignored (help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول3=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|العدد=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|عنوان=ignored (help) - ↑ G. L. C. M. van Rossen, H. van Bleiswijk: Über das Zustandsdiagramm der Kalium-Natriumlegierungen. In: Zeitschrift für anorganische Chemie. Band 74, 1912, S. 152–156; doi:10.1002/zaac.19120740115.
- ↑ . doi:10.1002/zaac.19120740115.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|عنوان=ignored (help) - ↑ Sobrasua Ibim. Biology: Threads of Life. Xlibris Corporation, 2010. صفحة 27. ISBN 1-4535-2068-6.. ISBN 1-4535-2068-6.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|صفحة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|مؤلف=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|المؤلف=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ Lawrie Ryan؛ Roger Norris. Cambridge International AS and A Level Chemistry Coursebook (الطبعة illustrated). Cambridge University Press, 2014. صفحة 36. ISBN 1-107-63845-3.. ISBN 1-107-63845-3.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|صفحة=ignored (help); Unknown parameter|طبعة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|مؤلف2=ignored (help); Unknown parameter|مؤلف=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الطبعة=تم تجاهله (مساعدة); الوسيط|المؤلف=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|المؤلف2=تم تجاهله (مساعدة); الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ Cowan، James A. (1997). Inorganic Biochemistry: An Introduction. Wiley-VCH. صفحة 7. ISBN 978-0-471-18895-7. OCLC 34515430.. ISBN 978-0-471-18895-7. OCLC 34515430.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help); Unknown parameter|وصلة=ignored (help)الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|الأول=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ De Leon، N. "Reactivity of Alkali Metals" Archived 2018-10-16 at the Wayback Machine. Indiana University Northwest. اطلع عليه بتاريخ 07 ديسمبر 2007.
{{cite web}}: Empty citation (help)الوسيط|تاريخ الوصول=تم تجاهله (مساعدة); الوسيط|الأول=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ Atkins، Peter W.؛ de Paula، Julio (2002). Physical Chemistry (الطبعة 7th). W. H. Freeman. ISBN 978-0-7167-3539-7. OCLC 3345182.. ISBN 978-0-7167-3539-7. OCLC 3345182.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير1=ignored (help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأول1=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|طبعة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الطبعة=تم تجاهله (مساعدة); الوسيط|الأول2=تم تجاهله (مساعدة); الوسيط|الأول1=تم تجاهله (مساعدة); الوسيط|الأخير1=تم تجاهله (مساعدة); الوسيط|الأخير2=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ Davies، Julian A. (1996). Synthetic Coordination Chemistry: Principles and Practice. World Scientific. صفحة 293. ISBN 978-981-02-2084-6. OCLC 717012347.. ISBN 978-981-02-2084-6. OCLC 717012347.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|الأول=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ P. E. Mason, F. Uhlig, V. Vaněk, T. Buttersack, S. Bauerecker, P. Jungwirth: Coulomb explosion during the early stages of the reaction of alkali metals with water. In: Nature chemistry. Band 7, Nummer 3, März 2015, S. 250–254, doi:10.1038/nchem.2161. پابميدPubMed.
- ↑ Habashi، Fathi. Alloys: Preparation, Properties, Applications. John Wiley & Sons, 2008. صفحات 278–280. ISBN 3-527-61192-4.. ISBN 3-527-61192-4.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|صفحات=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الصفحات=تم تجاهله (مساعدة); الوسيط|الأول=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ Lincoln، S.F.؛ Richens، D.T.؛ Sykes، A.G. (2004). "Metal Aqua Ions". Comprehensive Coordination Chemistry II. صفحة 515. ISBN 978-0-08-043748-4. doi:10.1016/B0-08-043748-6/01055-0."Metal Aqua Ions". doi:10.1016/B0-08-043748-6/01055-0. ISBN 978-0-08-043748-4.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير1=ignored (help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير3=ignored (help); Unknown parameter|الأول1=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول3=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|عنوان=ignored (help)الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الأول1=تم تجاهله (مساعدة); الوسيط|الأخير1=تم تجاهله (مساعدة); الوسيط|الأخير2=تم تجاهله (مساعدة); الوسيط|الأول3=تم تجاهله (مساعدة); الوسيط|الأخير3=تم تجاهله (مساعدة); الوسيط|الأول2=تم تجاهله (مساعدة); الوسيط|الصفحة=تم تجاهله (مساعدة) - ↑ Burgess، J. (1978). Metal Ions in Solution. New York: Ellis Horwood. ISBN 0-85312-027-7.. ISBN 0-85312-027-7.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|مكان=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|المكان=تم تجاهله (مساعدة); الوسيط|الأول=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ Starks، Charles M.؛ Liotta، Charles L.؛ Halpern، Marc (1994). Phase-Transfer Catalysis: Fundamentals, Applications, and Industrial Perspectives. Chapman & Hall. صفحة 162. ISBN 978-0-412-04071-9. OCLC 28027599.. ISBN 978-0-412-04071-9. OCLC 28027599.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير1=ignored (help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير3=ignored (help); Unknown parameter|الأول1=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول3=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|الأول3=تم تجاهله (مساعدة); الوسيط|الأخير3=تم تجاهله (مساعدة); الوسيط|الأول2=تم تجاهله (مساعدة); الوسيط|الأول1=تم تجاهله (مساعدة); الوسيط|الأخير1=تم تجاهله (مساعدة); الوسيط|الأخير2=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ Ivor L. Simmons (المحرر). Applications of the Newer Techniques of Analysis. Springer Science & Business Media, 2012. صفحة 160. ISBN 1-4684-3318-0.. ISBN 1-4684-3318-0.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|صفحة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|محرر=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|المحرر=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ Xu Hou (المحرر). Design, Fabrication, Properties and Applications of Smart and Advanced Materials (الطبعة illustrated). CRC Press, 2016. صفحة 175. ISBN 1-4987-2249-0.. ISBN 1-4987-2249-0.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|صفحة=ignored (help); Unknown parameter|طبعة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|محرر=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الطبعة=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|المحرر=تم تجاهله (مساعدة) - ↑ Nikos Hadjichristidis؛ Akira Hirao (المحررون). Anionic Polymerization: Principles, Practice, Strength, Consequences and Applications (الطبعة illustrated). Springer, 2015. صفحة 349. ISBN 4-431-54186-1.Akira Hirao (ed.). ISBN 4-431-54186-1.
{{cite book}}: Missing|editor1=(help); Missing or empty|title=(help); Unknown parameter|صفحة=ignored (help); Unknown parameter|طبعة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|محرر=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|المحرر=تم تجاهله (مساعدة); الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الطبعة=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ . doi:10.1021/ja00809a060.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير4=ignored (help); Unknown parameter|الأخير5=ignored (help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول4=ignored (help); Unknown parameter|الأول5=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|العدد=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|عنوان=ignored (help)Missing|last3=in Authors list (help) - ↑ Holleman، A. F.؛ Wiberg، E.؛ Wiberg، N. (2001). Inorganic Chemistry. Academic Press. ISBN 978-0-12-352651-9. OCLC 48056955.. ISBN 978-0-12-352651-9. OCLC 48056955.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير1=ignored (help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير3=ignored (help); Unknown parameter|الأول1=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول3=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الأول3=تم تجاهله (مساعدة); الوسيط|الأخير3=تم تجاهله (مساعدة); الوسيط|الأول2=تم تجاهله (مساعدة); الوسيط|الأول1=تم تجاهله (مساعدة); الوسيط|الأخير1=تم تجاهله (مساعدة); الوسيط|الأخير2=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ D. L. Ward, R. H. Huangj, J. L. Dye: The Structures of Alkalides and Electrides. III. Structure of Potassium Cryptand[2.2.2] Natride. In: Acta Cryst. C46, 1990, S. 1833–1835.
- ↑ Holleman، Arnold F.؛ Wiberg، Egon؛ Wiberg، Nils (1985). Lehrbuch der Anorganischen Chemie (باللغة German) (الطبعة 91–100). Walter de Gruyter. صفحات 931–943. ISBN 3-11-007511-3.. ISBN 3-11-007511-3.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير1=ignored (help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير3=ignored (help); Unknown parameter|الأول1=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول3=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صفحات=ignored (help); Unknown parameter|طبعة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|لغة=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الطبعة=تم تجاهله (مساعدة); الوسيط|الأخير3=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الأول1=تم تجاهله (مساعدة); الوسيط|اللغة=تم تجاهله (مساعدة); الوسيط|الأخير1=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الأول3=تم تجاهله (مساعدة); الوسيط|الأول2=تم تجاهله (مساعدة); الوسيط|الأخير2=تم تجاهله (مساعدة); الوسيط|الصفحات=تم تجاهله (مساعدة) صيانة CS1: لغة غير مدعومة (link). ISBN 3-11-007511-3.{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير1=ignored (help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير3=ignored (help); Unknown parameter|الأول1=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول3=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صفحات=ignored (help); Unknown parameter|طبعة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|لغة=ignored (help); Unknown parameter|ناشر=ignored (help) - ↑ قالب:OrgSynth
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 0-08-037941-9, p. 111
- ↑ Schumann، Walter (5 أغسطس 2008). Minerals of the World (الطبعة 2nd). Sterling. صفحة 28. ISBN 978-1-4027-5339-8. OCLC 637302667.. ISBN 978-1-4027-5339-8. OCLC 637302667.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|طبعة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الطبعة=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة); الوسيط|الأول=تم تجاهله (مساعدة); تحقق من التاريخ في:|date=(مساعدة) - ↑ . Bibcode:1977PhRvA..16.1507C. doi:10.1103/PhysRevA.16.1507.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير3=ignored (help); Unknown parameter|الأخير4=ignored (help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول3=ignored (help); Unknown parameter|الأول4=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|العدد=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|عنوان=ignored (help) - ↑ Dean، John Aurie؛ Lange، Norbert Adolph (1998). Lange's Handbook of Chemistry. McGraw-Hill. ISBN 0-07-016384-7.. ISBN 0-07-016384-7.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير1=ignored (help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأول1=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الأول2=تم تجاهله (مساعدة); الوسيط|الأخير2=تم تجاهله (مساعدة); الوسيط|الأخير1=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الأول1=تم تجاهله (مساعدة) - ↑ موسوعة رومب الكيميائية Römpp Lexikon Chemie, Georg Thieme Verlag
- ↑ . doi:10.1021/ja01386a008.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|العدد=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|عنوان=ignored (help) - ↑ F. Kögler: Die Bestimmung von Natrium als Natrium-Magnesium-Uranylacetat. In: Angewandte Chemie. 48, 1935, S. 561–565, doi:10.1002/ange.19350483403.
- ↑ Wissenschaft-Online-Lexika: Eintrag zu Natrium im Lexikon der Chemie.
- ↑ . PMID 13143043.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|العدد=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|مسار=ignored (help) - ↑ . PMID 7273405.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|العدد=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|مسار=ignored (help) - ↑ Srilakshmi، B. (2006). Nutrition Science (الطبعة 2nd). New Age International. صفحة 318. ISBN 978-81-224-1633-6. OCLC 173807260.. ISBN 978-81-224-1633-6. OCLC 173807260.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|طبعة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|مسار=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الطبعة=تم تجاهله (مساعدة); الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الأول=تم تجاهله (مساعدة); الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة) - ↑ Campbell، Neil (1987). Biology. Benjamin/Cummings. صفحة 795. ISBN 0-8053-1840-2.. ISBN 0-8053-1840-2.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الأول=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ P. Deetjen, E.-J. Speckmann, J. Hescheler: Physiologie. Elsevier, München 2005.
- ↑ McGuire، Michelle؛ Beerman، Kathy A. (2011). Nutritional Sciences: From Fundamentals to Food. Cengage Learning. صفحة 546. ISBN 978-0-324-59864-3. OCLC 472704484.. ISBN 978-0-324-59864-3. OCLC 472704484.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير1=ignored (help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأول1=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|الأول2=تم تجاهله (مساعدة); الوسيط|الأول1=تم تجاهله (مساعدة); الوسيط|الأخير1=تم تجاهله (مساعدة); الوسيط|الأخير2=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ W. Siegenthaler (Hrsg.): Klinische Pathophysiologie. 9. Auflage. Georg Thieme Verlag, Stuttgart 2006, ISBN 3-13-449609-7, S. 165–175.
- ↑ Pohl، Hanna R.؛ Wheeler، John S.؛ Murray، H. Edward (2013). المحررون: Astrid Sigel؛ Helmut Sigel؛ Roland K. O. Sigel. Interrelations between Essential Metal Ions and Human Diseases. Metal Ions in Life Sciences. 13. Springer. صفحات 29–47. doi:10.1007/978-94-007-7500-8_2.Helmut Sigel; Roland K. O. Sigel (eds.). Metal Ions in Life Sciences. doi:10.1007/978-94-007-7500-8_2.
{{cite book}}: Missing|editor1=(help); Missing or empty|title=(help); Unknown parameter|الأخير1=ignored (help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير3=ignored (help); Unknown parameter|الأول1=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول3=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صفحات=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|محرر=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الصفحات=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الأول3=تم تجاهله (مساعدة); الوسيط|الأخير3=تم تجاهله (مساعدة); الوسيط|الأول2=تم تجاهله (مساعدة); الوسيط|الأول1=تم تجاهله (مساعدة); الوسيط|المحرر=تم تجاهله (مساعدة); الوسيط|الأخير1=تم تجاهله (مساعدة); الوسيط|الأخير2=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ Müller-Esterl: Biochemie. Eine Einführung für Mediziner und Naturwissenschaftler. Spektrum Akademischer Verlag, 2004, ISBN 3-8274-0534-3.
- ↑ "Sodium and Potassium Quick Health Facts". health.ltgovernors.com.
{{cite web}}: Empty citation (help)الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|العمل=تم تجاهله (مساعدة) - ↑ "Sodium in diet". MedlinePlus, US National Library of Medicine. 5 اكتوبر 2016.
{{cite web}}: Empty citation (help)الوسيط|التاريخ=تم تجاهله (مساعدة); الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); تحقق من التاريخ في:|date=(مساعدة) - ↑ W. Kaim, B. Schwederski: Bioanorganische Chemie. 4. Auflage. Teubner, Wiesbaden 2005, ISBN 3-519-33505-0.
- ↑ "Sodium"(PDF). Northwestern University. تمت أرشفته من الأصل (PDF) فى 2011-08-23. اطلع عليه بتاريخ 21 نوفمبر 2011.
{{cite web}}: Empty citation (help)الوسيط|تاريخ الوصول=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|تاريخ الأرشيف=تم تجاهله (مساعدة); الوسيط|مسار الأرشيف=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|المسار=تم تجاهله (مساعدة) - ↑ Deutsche Gesellschaft für Ernährung e. V. Referenzwerte für die Nährstoffzufuhr. Abgerufen am 13. Dezember 2013.واي باك مشين Archived 2014-11-11 at the Wayback Machine
- ↑ World Health Organization: Global Strategy on Diet, Physical Activity and Health. Population sodium reduction strategies. Abgerufen am 13. Dezember 2013.واي باك مشين Archived 2018-04-18 at the Wayback Machine
- ↑ "Reference Values for Elements". Dietary Reference Intakes Tables. Health Canada.
{{cite web}}: Empty citation (help)الوسيط|الموقع=تم تجاهله (مساعدة); الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة) - ↑ . doi:10.1093/eurpub/14.3.235. PMID 15369026.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير3=ignored (help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول3=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|العدد=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|مسار=ignored (help) - ↑ . doi:10.1016/S0140-6736(08)60655-8. PMID 18456100.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير3=ignored (help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول3=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|العدد=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|عنوان=ignored (help) - ↑ Armstrong, James (2011). General, Organic, and Biochemistry: An Applied Approach. Cengage Learning. صفحات 48–. ISBN 1-133-16826-4.. ISBN 1-133-16826-4.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صفحات=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|مؤلف=ignored (help); Unknown parameter|مسار=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|المؤلف=تم تجاهله (مساعدة); الوسيط|الصفحات=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ "Sodium in Your Diet: Use the Nutrition Facts Label and Reduce Your Intake". US Food and Drug Administration. 2 يونيه 2016. اطلع عليه بتاريخ 15 اكتوبر 2016.
{{cite web}}: Empty citation (help)الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|تاريخ الوصول=تم تجاهله (مساعدة); الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|التاريخ=تم تجاهله (مساعدة); تحقق من التاريخ في:|access-date=, |date=(مساعدة) - ↑ "How much sodium should I eat per day?" Archived 2016-09-28 at the Wayback Machine. American Heart Association. 2016. اطلع عليه بتاريخ 15 اكتوبر 2016.
{{cite web}}: Empty citation (help)الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|تاريخ الوصول=تم تجاهله (مساعدة); الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|التاريخ=تم تجاهله (مساعدة); تحقق من التاريخ في:|access-date=(مساعدة) - ↑ P. Elliott, I. Brown: Sodium intakes around the world. Background document prepared for the Forum and Technical meeting on Reducing Salt Intake in Populations (Paris 5-7th October 2006).(PDF; 2,2 MB) 2006.واي باك مشين Archived 2017-10-14 at the Wayback Machine
- ↑ . doi:10.1016/S0140-6736(16)30467-6.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|عنوان=ignored (help) - ↑ Kering، M. K. (2008). "Manganese Nutrition and Photosynthesis in NAD-malic enzyme C4 plants Ph.D. dissertation" (PDF). University of Missouri-Columbia. اطلع عليه بتاريخ 09 نوفمبر 2011.
{{cite web}}: Empty citation (help)الوسيط|تاريخ الوصول=تم تجاهله (مساعدة); الوسيط|التاريخ=تم تجاهله (مساعدة); الوسيط|الأول=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ . doi:10.1080/07352680390243495.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير3=ignored (help); Unknown parameter|الأخير4=ignored (help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول3=ignored (help); Unknown parameter|الأول4=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|العدد=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|عنوان=ignored (help) - ↑ P. Sitte, E. W. Weiler u. a.: Strasburger. Lehrbuch der Botanik. 35. Auflage. Spektrum Akademischer Verlag, 2002, ISBN 3-8274-1010-X.
- ↑ K. Mengel: Ernährung und Stoffwechsel der Pflanze. 7. Auflage. Gustav Fischer Verlag, Jena 1991, ISBN 3-334-00310-8, S. 347–349.
- ↑ . doi:10.1016/S1360-1385(00)01838-0. PMID 11173290.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|العدد=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|عنوان=ignored (help) - ↑ "Plants and salt ion toxicity". Plant Biology. اطلع عليه بتاريخ 02 نوفمبر 2010.
{{cite web}}: Empty citation (help)الوسيط|تاريخ الوصول=تم تجاهله (مساعدة); الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة) - ↑ Remington، Joseph P. (2006). المحرر: Beringer، Paul. Remington: The Science and Practice of Pharmacy (الطبعة 21st). Lippincott Williams & Wilkins. صفحات 365–366. ISBN 978-0-7817-4673-1. OCLC 60679584.Beringer, Paul (ed.). ISBN 978-0-7817-4673-1. OCLC 60679584.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صفحات=ignored (help); Unknown parameter|طبعة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الطبعة=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الصفحات=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة); الوسيط|الأول=تم تجاهله (مساعدة) - ↑ Alfred Klemm, Gabriele Hartmann, Ludwig Lange, "Sodium and Sodium Alloys" in Ullmann's Encyclopedia of Industrial Chemistry 2005, Wiley-VCH, Weinheim. doidoi:10.1002/14356007.a24_277
- ↑ K. Ziegler, F. Bersch, H. Wollthan: Untersuchungen über alkaliorganische Verbindungen. XI. Der Mechanismus der Polymerisation ungesättigter Kohlenwasserstoffe durch Alkalimetalle und Alkalialkyle. In: Justus Liebigs Annalen der Chemie. 511, 1, 1934, S. 13–44; doi:10.1002/jlac.19345110103.
- ↑ Deutsches Chemie-Museum Merseburg, Geschichte der Busa-Werke Schkopau.واي باك مشين Archived 2017-04-29 at the Wayback Machine
- ↑ "Sodium-cooled Fast Reactor (SFR)" (PDF). Office of Nuclear Energy, U.S. Department of Energy. 18 فبراير 2015.
{{cite web}}: Empty citation (help)الوسيط|التنسيق=تم تجاهله (مساعدة); الوسيط|التاريخ=تم تجاهله (مساعدة); الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|العمل=تم تجاهله (مساعدة); تحقق من التاريخ في:|date=(مساعدة) - ↑ Sodium as a Fast Reactor Coolant presented by Thomas H. Fanning. Nuclear Engineering Division. U.S. Department of Energy. U.S. Nuclear Regulatory Commission. Topical Seminar Series on Sodium Fast Reactors. May 3, 2007
- ↑ M. Volkmer: Basiswissen Kernenergie. Hamburgische Elektricitäts-Werke-AG, 1996, ISBN 3-925986-09-X, S. 52–53.
- ↑ Fire and Explosion Hazards. Research Publishing Service, 2011. صفحة 363. ISBN 981-08-7724-2.. ISBN 981-08-7724-2.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|صفحة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة) - ↑ Pavel Solomonovich Knopov, Panos M. Pardalos (المحررون). Simulation and Optimization Methods in Risk and Reliability Theory. Nova Science Publishers, 2009. صفحة 150. ISBN 1-60456-658-2.. ISBN 1-60456-658-2.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|editors=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) صيانة CS1: يستخدم وسيط المحررون (link). ISBN 1-60456-658-2.{{cite book}}: Missing or empty|title=(help); Unknown parameter|editors=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help) - ↑ McKillop، Allan A. Proceedings of the Heat Transfer and Fluid Mechanics Institute. Stanford University Press, 1976. صفحة 97. ISBN 0-8047-0917-3.. ISBN 0-8047-0917-3.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|السنة=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help); Unknown parameter|وصلة=ignored (help)الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|الأول=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ U.S. Atomic Energy Commission. Reactor Handbook: Engineering (الطبعة 2). Interscience Publishers. صفحة 325.
{{cite book}}: Empty citation (help)الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|المؤلف=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الطبعة=تم تجاهله (مساعدة) - ↑ A US US2949907 A, Tauschek Max J, "Coolant-filled poppet valve and method of making same", published 23 Aug 1960A US US2949907 A, قالب:Cite patent/authors, "Coolant-filled poppet valve and method of making same", published 23 Aug 1960
- ↑ Lindsey، Jack L. (1997). Applied illumination engineering. Fairmont Press. صفحات 112–114. ISBN 978-0-88173-212-2. OCLC 22184876.. ISBN 978-0-88173-212-2. OCLC 22184876.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صفحات=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|مسار=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الصفحات=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة); الوسيط|الأول=تم تجاهله (مساعدة) - ↑ Sethi، Arun (1 يناير 2006). Systematic Laboratory Experiments in Organic Chemistry. New Age International. صفحات 32–35. ISBN 978-81-224-1491-2. OCLC 86068991.. ISBN 978-81-224-1491-2. OCLC 86068991.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صفحات=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|مسار=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الصفحات=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة); الوسيط|الأول=تم تجاهله (مساعدة); تحقق من التاريخ في:|date=(مساعدة) - ↑ R. Brückner: Reaktionsmechanismen. 3. Auflage. Spektrum Akad. Verlag, 2004, ISBN 3-8274-1579-9.
- ↑ Smith، Michael. Organic Synthesis (الطبعة 3). Academic Press, 2011. صفحة 455. ISBN 0-12-415884-6.. ISBN 0-12-415884-6.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|طبعة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الطبعة=تم تجاهله (مساعدة); الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|الأول=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ Solomons & Fryhle. Organic Chemistry (الطبعة 8). John Wiley & Sons, 2006. صفحة 272. ISBN 81-265-1050-1.. ISBN 81-265-1050-1.
{{cite book}}: Cite uses deprecated parameter|authors=(help); Missing or empty|title=(help); Unknown parameter|صفحة=ignored (help); Unknown parameter|طبعة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الطبعة=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) صيانة CS1: يستخدم وسيط المؤلفون (link). ISBN 81-265-1050-1.{{cite book}}: Cite uses deprecated parameter|authors=(help); Missing or empty|title=(help); Unknown parameter|صفحة=ignored (help); Unknown parameter|طبعة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help) - ↑ Lerner، Leonid (2011-02-16). Small-Scale Synthesis of Laboratory Reagents with Reaction Modeling. CRC Press. صفحات 91–92. ISBN 978-1-4398-1312-6. OCLC 669160695.. ISBN 978-1-4398-1312-6. OCLC 669160695.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صفحات=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|مسار=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الأول=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة); الوسيط|الصفحات=تم تجاهله (مساعدة) - ↑ Angelici, R. J. (1999). Synthesis and Technique in Inorganic Chemistry. Mill Valley, CA: University Science Books. ISBN 0-935702-48-2.. ISBN 0-935702-48-2.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|مؤلف=ignored (help); Unknown parameter|مكان=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|المؤلف=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ Routley، J. Gordon. Sodium Explosion Critically Burns Firefighters: Newton, Massachusetts. U. S. Fire Administration. FEMA, 2013.
{{cite book}}: Empty citation (help)الوسيط|الأول=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة) - ↑ Prudent Practices in the Laboratory: Handling and Disposal of Chemicals. National Research Council (U.S.). Committee on Prudent Practices for Handling, Storage, and Disposal of Chemicals in Laboratories. National Academies, 1995. صفحة 390.
{{cite book}}: Empty citation (help)الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة) - ↑ "Sodium and Salt". www.heart.org. اطلع عليه بتاريخ 05 سبتمبر 2016.
{{cite web}}: Empty citation (help)الوسيط|الموقع=تم تجاهله (مساعدة); الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|تاريخ الوصول=تم تجاهله (مساعدة) - ↑ Ladwig، Thomas H. Industrial fire prevention and protection. Van Nostrand Reinhold, 1991. صفحة 178. ISBN 0-442-23678-6.. ISBN 0-442-23678-6.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|ناشر=ignored (help)الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|الأول=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الأخير=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة) - ↑ Günter Kessler. Sustainable and Safe Nuclear Fission Energy: Technology and Safety of Fast and Thermal Nuclear Reactors (الطبعة illustrated). Springer Science & Business Media, 2012. صفحة 446. ISBN 3-642-11990-5.. ISBN 3-642-11990-5.
{{cite book}}: Missing or empty|title=(help); Unknown parameter|السنة=ignored (help); Unknown parameter|صفحة=ignored (help); Unknown parameter|طبعة=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|مؤلف=ignored (help); Unknown parameter|ناشر=ignored (help); Unknown parameter|وصلة=ignored (help)الوسيط|الصفحة=تم تجاهله (مساعدة); الوسيط|المؤلف=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|الطبعة=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة)
بلغات أجنبية[تعديل]
لينكات برانيه[تعديل]
- الصوديوم فى فيديوهات الجدول الدوري (من جامعة نوتنجهام)
- أصل كلمة "natrium" – مصدر الرمز Na
- ↑ "القلويات" Archived 2022-11-12(Date mismatch) at the Wayback Machine. الموسوعة العربية.
{{cite web}}: Empty citation (help)الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة) - ↑ "سلسلة العناصر المعدنية - الصوديوم". الباحثون السوريون. 08 أبريل 2016.
{{cite web}}: Empty citation (help)الوسيط|التاريخ=تم تجاهله (مساعدة); الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); تحقق من التاريخ في:|date=(مساعدة) - ↑ "صوديوم اقل وبوتاسيوم أكثر". موقع الطبي.
{{cite web}}: Empty citation (help)الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة) - ↑ "اختبار الصوديوم" Archived 2016-12-01 at the Wayback Machine. موسوعة الملك عبد الله بن عبد العزيز العربية للمحتوى الصحي. 01.10.2011.
{{cite web}}: Empty citation (help)الوسيط|التاريخ=تم تجاهله (مساعدة); الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|الناشر=تم تجاهله (مساعدة); تحقق من التاريخ في:|date=(مساعدة) - ↑ "استخدامات الصوديوم". كيمياء العناصر، المجموعة الأولى: القلويات. المدرسة العربية. اطلع عليه بتاريخ 7 يناير 2012.
{{cite web}}: Empty citation (help)الوسيط|الناشر=تم تجاهله (مساعدة); الوسيط|تاريخ الوصول=تم تجاهله (مساعدة); الوسيط|المسار=تم تجاهله (مساعدة); الوسيط|العنوان=تم تجاهله (مساعدة); الوسيط|العمل=تم تجاهله (مساعدة); تحقق من التاريخ في:|access-date=(مساعدة)









